Da un anno il Consiglio Europeo per la Salute ha deciso di aumentare l’offerta di screening contro il cancro.[1] Oltre a quelli per cancro mammario (cui la United States Preventive Services Task Force/USPSTF ha di recente esteso l’offerta a partire dai 40 anni, suscitando controversie),[2] per cervice uterina e colon-retto, gli Stati membri hanno convenuto di ampliare gli screening a:
- carcinoma polmonare, esaminando la fattibilità e l’efficacia dell’uso della tomografia computerizzata (TC) spirale a bassa dose;
- carcinoma prostatico, già oggetto di diffusi screening opportunistici, valutando fattibilità ed efficacia di programmi organizzati;
- carcinoma gastrico, da considerare in paesi e regioni con tassi d’incidenza e mortalità specifici elevati.
Ritengo che il potenziamento di screening tumorali, fatti oggetto di offerta e propaganda estesa o universale, configuri politiche di sanità pubblica molto discutibili e comunque non certo prioritarie. Infatti, oltre ad aumentare i carichi di lavoro e i costi per i sistemi sanitari, ciò aumenta sovra-diagnosi, interventi invasivi e loro possibili complicanze, e non riduce affatto la mortalità totale, contrariamente a una diffusa convinzione. In questo contributo documenterò l’affermazione sia in generale, sia con gli esempi specifici di screening per un paio di tumori: quello più diffuso nel sesso femminile, e quello più letale.
Un’indagine meta-epidemiologica del 2015 sugli studi randomizzati controllati (RCT) disponibili aveva già documentato che gli screening tumorali non salvano vite,[3] e una rassegna Cochrane del 2019 lo aveva confermato in generale per gli screening sanitari (health checks), e nello specifico per quelli tumorali, come sintetizzano le slide sotto riportate.[4]


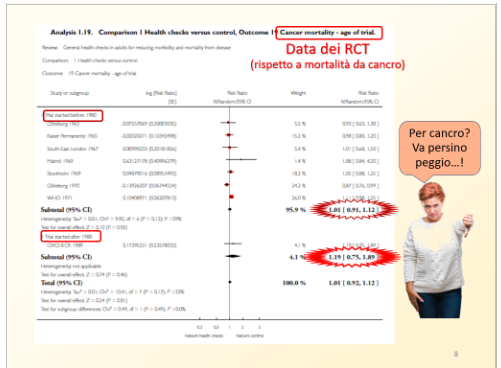
Gli screening tumorali, in particolare, non mostrano alcuna tendenza al miglioramento degli esiti nei RCT più recenti, ma al contrario una tendenza a esiti peggiori, forse spiegabile con l’aumento delle sovra-diagnosi, dei trattamenti non necessari e delle loro conseguenze con l’impiego di test di screening via via sempre più sensibili.
L’ultima in ordine di tempo delle metanalisi sul tema conferma che “le prove correnti non supportano l’affermazione che i comuni test di screening tumorali salvino vite estendendone la durata, forse con l’eccezione dello screening del tumore colorettale con sigmoidoscopia”.[5]
Screening mammografico del cancro mammario
Peter Gotzsche, primo autore della celebre rassegna Cochrane sullo screening del cancro mammario,[6] espulso dalla Cochrane con una vera “congiura di palazzo” che anche i NoGrazie hanno stigmatizzato con una dura presa di posizione,[7] ha di recente aggiornato la rassegna al 10 gennaio 2023.[8] Quanto emerge dai dati è una lieve progressiva tendenza all’aumento della mortalità totale (per cause diverse dal tumore mammario) con il proseguimento dei follow-up, potenzialmente compatibile con l’accumulo di danni legati all’eccesso di terapie non necessarie cui sono sottoposte le molte pazienti sovra-diagnosticate.[9,10] Alla disturbante tendenza all’aumento di mortalità non tumorale si accompagna un significativo aumento di tumorectomie e mastectomie, che sollevano dubbi sulla razionalità della scelta di sottoporsi a questo screening, e potrebbero mettere in discussione l’opportunità di proseguire con un’offerta di screening mammografico non mirata.


Screening del cancro polmonare con TC spirale a bassa dose
L’USPSTF, e a seguire altre Agenzie sanitarie e Società professionali, ha raccomandato lo screening in oggetto,[11] dapprima nei fumatori con le caratteristiche dei partecipanti al grande RCT USA NLST;[12] poi esteso a partire dai 50 anni (anziché 55) e con solo 20 (anziché 30) pacchetti-anno totali di fumo di sigaretta.[13] Poi, con un déjà vu, con richieste di fare molto di più,[14] fino a ipotesi di estendere lo screening a non fumatori.[15]
Purtroppo, però, come in genere accade anche per altri screening, si lascia di fatto intendere che la riduzione di mortalità specifica (per ca polmonare) conseguita si traduca in una riduzione di mortalità totale. All’equivoco ha contribuito anche il grande NLST,[12] in cui però due fattori che possono aver contribuito a una riduzione (pur non statisticamente significativa) della mortalità totale. Il primo è un gruppo di controllo con soggetti che ricevevano una radiografia (Rx) del torace, che potrebbe non essere affatto associata a riduzione di mortalità; il secondo, più importante, è la localizzazione negli USA. Infatti, anche nella rassegna Cochrane sugli health checks,[4] i RCT negli USA si associano di norma a risultati meno deludenti rispetto a quelli Europei, forse perché l’assenza di SSN, o comunque di coperture sanitarie generali e medicina di base, fa sì che per molti cittadini USA partecipare a un RCT sia l’occasione per esser sottoposti a un iter diagnostico (che identifica anche condizioni sanitarie trattabili), che invece in Europa di norma è assicurato al bisogno dalle cure primarie.
Quando invece si considera una metanalisi dei RCT che hanno confrontato la TC spirale con placebo,[16, Fig. 1B] i risultati, non significativi, sulla mortalità totale presentano intervalli di confidenza piuttosto ampi: RR 0,98 (0,90-1,07). Soprattutto, però, nel solo RCT europeo di dimensioni adeguate, che è anche l’unico nella metanalisi valutato a basso rischio di bias,[16, Fig. A3] il danese DLCST, il risultato va in direzione opposta: RR 1,46 (0,99-2,14, che sfiora la significatività statistica) per la mortalità totale, con 61 morti con TC spirale contro 42 nel gruppo placebo; e 1,36 (0,63-2,96) per la mortalità correlata al ca polmonare.
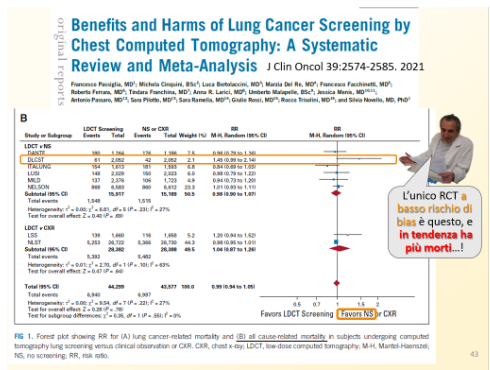
Non basta. La recente pubblicazione di uno studio osservazionale con l’esplicito obiettivo di quantificare l’entità della cascata di procedure e complicazioni associate alla TC spirale di screening, ha confermato l’ipotesi di molti critici, che nel mondo reale tali conseguenze siano ben maggiori di quanto si registra nei RCT, dove ciò che segue agli screening è di regola assicurato in centri d’élite.[17] Nei soggetti screenati si è infatti registrato un 15,9% di anormalità rilevate nella TC di screening, con un ~32% di accertamenti diagnostici (di norma con TC ad alta risoluzione e alte dosi di radiazioni ionizzanti) e un 2,8% di procedure invasive, con tasso di complicazioni sostanzialmente più alto di quanto rilevato nel NLST:[12] qualsiasi complicazione 30,6% vs 17,7%, complicazioni maggiori 20,6% vs 9,4%.
Poiché negli esempi considerati (per i restanti screening si rimanda ad altra occasione) non c’è alcun vantaggio per la mortalità totale, esito cui la maggioranza degli assistiti informati darebbe priorità, c’è da chiedersi perché anche la Sanità pubblica si accanisca nell’offrire/estendere questi screening, anziché privilegiare interventi (per la cessazione dal fumo, prescrizione di attività fisica, educazione/prescrizione di modelli alimentari salutari, de-prescrizione farmacologica…) in cui i benefici per la mortalità e la morbosità sono invece ben provati, come pure la riduzione dei costi per i servizi sanitari. La risposta è purtroppo ovvia: chi detiene il potere in Sanità (grandi produttori ed erogatori con i correnti modelli di remunerazione, e Regolatori e Politica da questi catturati) non ha alcun interesse a ridurre i costi (cioè le proprie entrate!) e le opportunità di lavoro per le proprie produzioni/discipline, e promuoverà gli screening, non stili di vita e abbandono di prestazioni iatrogene. Inoltre. oggi il mantra che la mortalità post-pandemica non si sta riducendo per insufficienti screening (!) è un buon pretesto per non rivolgere l’attenzione ad altri fattori e responsabilità, mentre si continua a fare/ampliare i propri business. È arduo uscirne, senza una riforma paradigmatica dei modelli di finanziamento e remunerazione degli attori in Sanità che renda per loro conveniente la Salute, anziché le prestazioni/le malattie,[18] com’è di fatto oggi.
Alberto Donzelli
1. Consiglio dell’Unione Europea. Raccomandazione del Consiglio relativa al rafforzamento della prevenzione attraverso l’individuazione precoce: un nuovo approccio dell’UE allo screening dei tumori, che sostituisce la raccomandazione 2003/878/CE del Consiglio. 29 nov 2022 allegato1670747147.pdf (quotidianosanita.it)
2. Woloshin S, Jørgensen KJ, Hwang S et al. The New USPSTF Mammography Recommendations – A Dissenting View. N Engl J Med 2023 Sep 21;389(12):1061-1064. doi:10.1056/NEJMp2307229
3. Saquib N, Saquib J, Ioannidis JP. Does screening for disease save lives in asymptomatic adults? Systematic review of meta-analyses and randomized trials. Int J Epidemiol 2015;44(1):264-77. doi: 10.1093/ije/dyu140
4. Krogsbøll LT, Jørgensen KJ, Gøtzsche PC. General health checks in adults for reducing morbidity and mortality from disease. Cochrane Database Syst Rev 2019 Jan 31;1(1):CD009009. doi: 10.1002/14651858.CD009009.pub3
5. Bretthauer M, Wieszczy P, Løberg M et al. Estimated Lifetime Gained With Cancer Screening Tests. A Meta-Analysis of Randomized Clinical Trials. JAMA Intern Med 2023 doi:10.1001/jamainternmed.2023.3798
6. Gøtzsche PC, Jørgensen KJ. Screening for breast cancer with mammography. Cochrane Database Syst Rev 2013 Jun 4;2013(6):CD001877. doi: 10.1002/14651858.CD001877.pub5
7. Newsletter NoGrazie n. 63 – Ottobre 2018 – https://facebook.com/pages/NoGraziePagoIo/180764791950999
8. Gotzsche P. Institute for Scientific Freedom. Publications – Institute for Scientific Freedom
9. Donzelli A. The benefits and harms of breast cancer screening: an independent review. Lancet 2013 Mar 9;381:799-800. doi:10.1016/S0140-6736(13)60619-4
10. Donzelli A, Giudicatti G, Sghedoni D. Mammography screening for breast cancer: the UK Age trial. Lancet Oncol 2020 Nov;21(11):e509. doi: 10.1016/S1470-2045(20)30631-8
11. Moyer VA, U.S. Preventive Services Task Force. Screening for lung cancer: U.S. Preventive Services Task Force recommendation statement. Ann Intern Med 2014;160:330-338
12. Aberle DR, Adams AM, Berg CD et al: National Lung Screening Trial Research Team. Reduced lung-cancer mortality with low-dose computed tomographic screening. N Engl J Med 2011;365:395-409
13. US Preventive Services Task Force. Screening for lung cancer: US Preventive Services Task Force recommendation statement. JAMA Published online March 9, 2021. doi:10.1001/jama.2021.1117
14. Ito Fukunaga M, Wiener RS, Slatore CG. The 2021 US Preventive Services Task Force Recommendation on Lung Cancer Screening: The More Things Stay the Same. JAMA Oncol 2021;7(5):684–686. doi:10.1001/jamaoncol.2020.8376
15. Gao W, Wen CP, Wu A, Welch HG. Association of Computed Tomographic Screening Promotion With Lung Cancer Overdiagnosis Among Asian Women. JAMA Intern Med 2022 Mar 1;182(3):283-290. doi: 10.1001/jamainternmed.2021.7769
16. Passiglia F, Cinquini M, Bertolaccini L et al. Benefits and Harms of Lung Cancer Screening by Chest Computed Tomography: A Systematic Review and Meta-Analysis. J Clin Oncol 2021;39(23):2574-2585. doi: 10.1200/JCO.20.02574.
17. Rendle KA, Saia CA, Vachani A et al. Rates of Downstream Procedures and Complications Associated With Lung Cancer Screening in Routine Clinical Practice: A Retrospective Cohort Study. Ann Intern Med 2024 Jan;177(1):18-28. doi: 10.7326/M23-0653
18. Donzelli A. Una riforma strutturale per la sanità: pagare la salute, non la malattia. Allineare le convenienze dei diversi attori all’etica e alla salute della comunità dei cittadini. Cap. 14 del libro Un nuovo mo(n)do per fare salute. Le proposte della Rete Sostenibilità e Salute. Celid 2019, Torino. Cap. 14 del libro Un nuovo mo(n)do per fare salute. Le proposte della Rete Sostenibilità e Salute. | Fondazione Allineare Sanità e Salute (fondazioneallinearesanitaesalute.org)