Il New England Journal of Medicine ha pubblicato i risultati del RCT condotto da Pfizer sugli adolescenti tra 12 e 15 anni di età (1). Il reclutamento ha avuto luogo tra ottobre e gennaio 2020 solo negli USA, come parte dello studio multicentrico sugli adulti a partire dai 16 anni, condotto anche in altri paesi e che abbiamo analizzato nella lettera di gennaio 2021 (2). La tabella riassume i risultati principali.
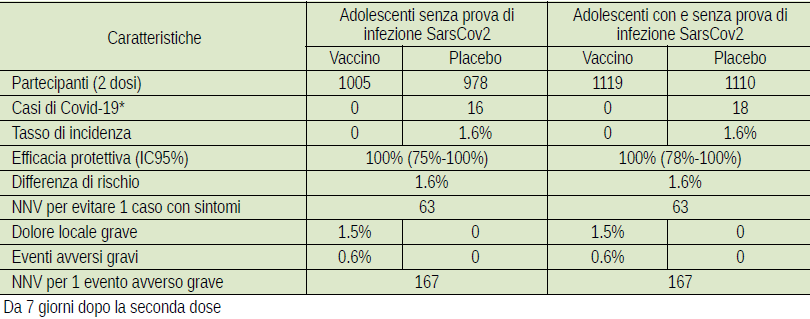
Anche questo RCT è stato organizzato dalla ditta produttrice e gli autori riportano numerosi conflitti di interessi (CdI). Il campione è quasi 20 volte più piccolo rispetto allo studio sugli adulti, per cui gli intervalli di confidenza al 95% per l’efficacia protettiva sono più ampi. Per la stessa ragione, e per la breve durata dell’osservazione (conclusa il 31 marzo 2021), non ci sono risultati per molti esiti di interesse, ma rari: malattia grave, ricoveri, decessi, reazioni allergiche gravi ed eventi avversi tardivi. La stima del NNV (number needed to vaccinate, cioè il numero di adolescenti da vaccinare per evitare un caso di Covid-19) è circa la metà rispetto a quella degli adulti, ma anche per questo indicatore gli intervalli di confidenza sono probabilmente molto ampi (e impossibili da calcolare con i dati forniti). Come per il RCT sugli adulti, non ci sono dati sulle infezioni evitate, e cioè sui possibili effetti della vaccinazione sulla trasmissione del virus.
Mancano ovviamente dati sull’efficacia protettiva in caso di varianti del virus e sulla durata dell’immunità.
La sicurezza a breve termine in questa fascia di età sembra essere molto simile a quella riportata negli adulti.
Molto frequenti le reazioni locali (soprattutto dolore, ma anche gonfiore e arrossamento), ma poche quelle considerate gravi; in media della durata di 1-2 giorni. Frequenti anche le reazioni avverse sistemiche, soprattutto affaticamento, cefalea, brividi e dolori muscolari, ma quelle classificate come gravi, dalle barre degli istogrammi, sembrano di pochi punti percentuali. Anche per le reazioni sistemiche la durata media dichiarata dagli autori è di 1-2 giorni.
Nel frattempo, il sito dell’AAAS (American Association for the Advancement of Science) riferisce che un gruppo di ricercatori israeliani ha inviato il 1 Giugno 2021 al Ministero della Salute un’allerta su un possibile eccesso di casi di miocardite in maschi tra 16 e 24 anni di età vaccinati con Pfizer (3). Si tratterebbe di un caso su 3000-6000 vaccinati, ma provenendo i dati da un sistema di sorveglianza passiva, i tassi reali, stimabili solo con sorveglianza attiva, potrebbero essere più elevati. Tutti i casi riportati, circa 100 in questa fascia di età, erano lievi e sono andati incontro a risoluzione spontanea o con terapia antinfiammatoria. Casi simili, ma in numero minore, sono stati riportati anche negli USA (4). Nel suo bollettino dell’11 Giugno, l’EMA riporta 122 casi di miocardite, uno su 160mila dosi di vaccino Pfizer somministrate (5); ma in Europa sono pochi, in relazione a Israele, i maschi vaccinati nella fascia di età che sembra essere colpita. Dato che il RCT del vaccino Pfizer sugli adolescenti ha interessato poco più di 1000 soggetti, è impossibile dire quale sia il rischio di miocardite post-vaccinale tra i ragazzi di 12-15 anni di età.
Da notare inoltre che il Centro Europeo per il Controllo delle Malattie (ECDC), in un rapporto tecnico diffuso il 1 Giugno 2021, scrive che, considerato il probabile basso rapporto tra benefici e rischi per i singoli individui di età compresa tra 12 e 15 anni, in comparazione con adulti e anziani, ci dovrebbe essere un’attenta considerazione della situazione epidemiologica, compresi i tassi di copertura nei gruppi prioritari (anziani, adulti, “fragili”), prima di decidere di includere gli adolescenti tra i target del programma di vaccinazioni (6). Infine, segnaliamo che l’OMS afferma che “non è necessario che gli alunni siano vaccinati prima che possano ritornare a scuola”(7).
Adriano Cattaneo
1. Frenck RWJr, Klein NP, Kitchin N et al. Safety, immunogenicity, and efficacy of the BNT162b2 Covid-19 vaccine in adolescents. NEJM May 27, 2021 DOI: 10.1056/NEJMoa2107456
2 Polack FP, Thomas SJ, Kitchin N, et al. Safety and efficacy of the BNT162b2 mRNA Covid-19 vaccine. N Engl J Med 2020; 383: 2603-15